[인텔리아 테라퓨틱스, NTLA] 유전자 가위 유전자 편집 치료 혁신 기업

오늘 공부할 기업은 유전자 가위, 유전자 편집 치료 혁신 기업 중 하나인 인텔리아 테라퓨틱스, NTLA이다.
1. 기업소개
Sector : Biotechnology
Industry : Health Care/Life Sciences
2014년 설립된 크리스퍼 유전자 가위 기업. 시리즈a 투자자로 Novartis가 참여하여 1,500만 달러를 투자받았으며, 2016년 나스닥에 상장했다. Crispr/Cas9 복합체의 각 전달을 위한 바이러스 벡터 대비 많은 양의 유전자 치료제 적재 능력과 낮은 면역원성을 갖춘 지질나노입자 (LNP)의 유용성에 대한 연구와 면역항암 분야 및 자가면역 치료 분야에 대한 유전자 가위 적용 법을 연구 중인 기업이다.


2020년 노벨화학상은 최신 유전자 편집 기술인 크리스퍼 유전자 가위(CRISPR-Cas9)를 주도적으로 연구한 프랑스의 에마뉘엘 샤르팡티에(51)와 미국의 제니퍼 A 다우드나(56)에게 돌아갔다. 노벨 화학상 수상장인 두 명의 여성 과학자가 힘을 합쳤으면 좋았겠지만, 사진상 왼쪽에 있는 미국의 재니퍼 A 다우드나 교수는 NTLA, 인텔리아 테라퓨틱스를 우측의 마뉘엘 샤르팡티에 교수는 CRSP, 크리스퍼 테라퓨틱스를 각각 설립하게 되었다.
2. CRISPER/CAS9 기술이란?
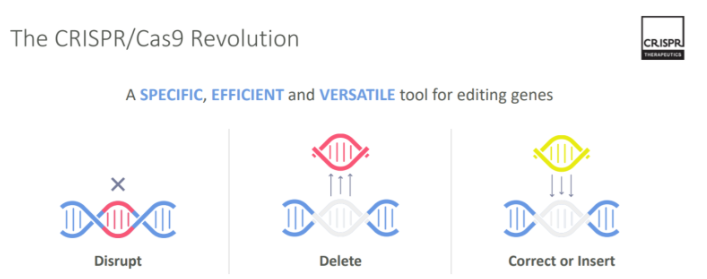
3세대 유전자 가위인 크리스퍼 기술로 쉽게 유전자 가위라고 부른다. 유전 정보를 담고 있는 DNA를 가위처럼 편집을 하여 유전 정보를 수정 또는 삭제하거나 새로운 유전 정보를 삽입할 수 있다.
기전은 DNA의 일부 염기를 바꾸여 유전 서열을 바꾸는 DISRUPT, 일부를 삭제하는 DELETE, 새로운 유전 정보를 삽입하는 CORRECT/INSERT 가 있다.
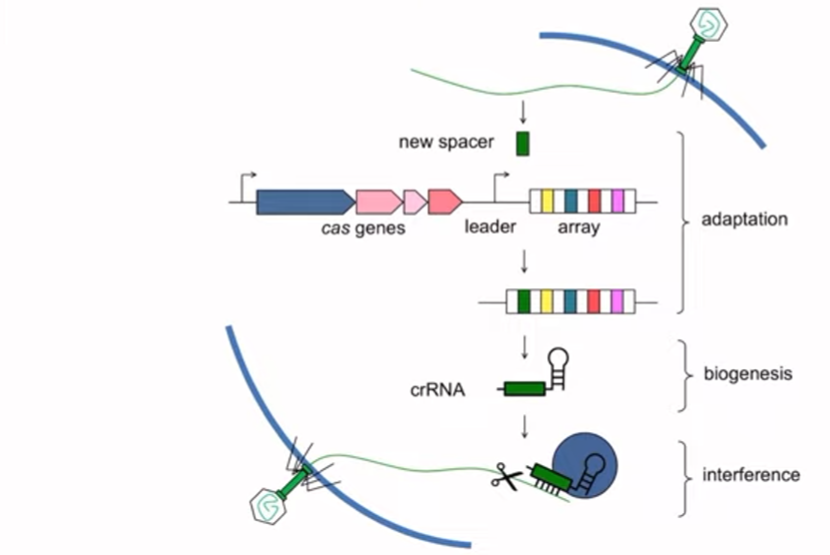
이 기술은 세균이 바이러스로부터 세균 스스로를 보호하기 위한 기전이다. 바이러스는 세균에게 유전체를 밀어넣어 자기가 필요한 것을 세균을 통해서 만들게끔 하고 결국에는 세균을 깨고 나와버린다. 그렇기 때문에 세균은 죽지 않으려면 이 바이러스 유전체를 없애 버려야 한다. 이러한 유전체를 없애기 위해 크리스퍼진에 바이러스 유전체 일부 표식자(new spacer)를 넣어두는 것이다. 동일한 바이러스가 다시 들어왔다 라고 하면 이 크리스퍼진에서 가이드 RNA를 만들고 CAS9라는 유전자 가위와 같이 결합하여 이 유전체를 편집하는 것이다.
하기 영상은 유전자 편집 기술이 유전자에 어떻게 적용되는지 보여주는 TED 영상이다.
https://www.youtube.com/watch?v=6tw_JVz_IEc

인텔리아 테라퓨틱스 기술의 핵심은 유전자 가위 역할을 수행할 Crispr/Cas9 단백질을 직접 체내 타겟 세포까지 지질나노입자를 통해 전달하고, 돌연변이가 발생한 유전자를 Knock-out 시키거나 복구, 혹은 연속적인 두 과정을 모두 포함된 연속적 편집을 수행하는 기술, 그리고 면역 항암치료와 자가면역치료를 위해 Crispr 엔지니어링 플랫폼을 활용하여 체외에서 유전자 조작한 세포를 직접 치료제로써 활용하는 기술이라고 볼 수 있다.
3. NTLA, 인텔리아 테라퓨틱스 파이프라인

인텔리아의 파이프라인은 크리스퍼 가위를 직접 체내에 주입하여 반영구적으로 휘귀 유전병을 치료하는 In Vivo 파이프라인과 체외에서 유전자 조직을 거친 세포를 주입하여 면역 항암 및 자가면역 질환을 치료하는 Ex Vivo 파이프라인으로 나누어진다.
In-Vivo 방식의 경우 유전자 가위를 환자에게 직접 체내에 주입함으로써 Ex-Vivo처럼 환자의 세포를 추출, 형질전환, 배양 등의 체외 조작이 필요가 없어 유전자가위 형성에 필요한 준비시간과 비용을 줄일 수 있는 장점이 있다. 그러나, 완성되지 않는 불안정한 치료제를 몸에 투여하는 것이기 때문에 표적 이탈과 인체 내에서 면역 반응을 유발하여 부작용을 일으킬 단점이 있다.
Ex-Vivo의 경우 환자로부터 전달 세포를 채취하고 치료용 유전자가 삽입된 바이러스를 도입하여 체외에서 치료 목적의 유전자 가위를 만들어 체내에 투여한다. 이 방법은 목표로 하는 장기나 조직세포 이외에 무작위 하게 반응하여 생기는 부작용을 줄일 수 있는 장점이 있으나, 해당 치료법을 적용할 수 있는 질병들이 제한적이며 In-Vivo 방식 대비 시간과 비용 측면에서 단점이 있다.
Ex Vivo 의 선두기업은 CRSP, 크리스퍼 테라퓨틱스이며 In Vivo의 선두주자가 NTLA, 인텔리아 테라퓨틱스이다.


NTLA, 인텔리아는 In Vivo와 Ex vivo 두 가지 기술을 모두 가지고 있으며 특히, In Vivo의 핵심 기술력인 LNP라는 Lipid Nanoparticle의 형태로 Mrna를 보호할 수 있는 자체 기술력이 있다. 크리스퍼 테라퓨틱스의 경우 LNP 자체 기술력이 없다.

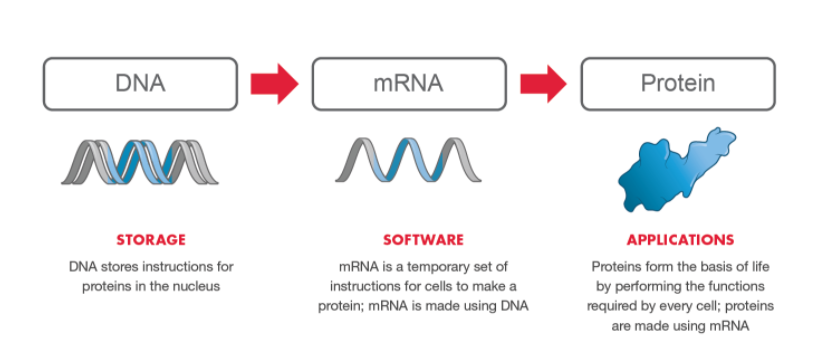
유전체인 DNA 바로 단백질이 될 수 없으며 MRNA를 거쳐서 단백질이 될 수 있다. 단백질은 생체 활동의 가장 기본이 되는 단위이다. DNA가 STORAGE면 MRNA는 SOFTWARE가 되어 단백질인 APPLICATIONS을 만드는 것이다.
이러한 MRNA는 우리 몸에다가 주입을 하게 되면 불안정하여 쉽게 분해가 되기 때문에 표적 장기로 도달하기가 어렵다. 이 MRNA를 감싸줄 수 있는 보호막이 필요한데, 이 보호막이 바로 LNP기술이다.

지금 개발되어 우리가 접종하고 있는 코로나 백신도 MRNA백신이다. 화이자와 모더나 역시 LNP 자체 기술을 보유하고 있기 때문에 불안정한 MRNA를 감싸서 코로나 백신을 개발할 수 있었다.

인텔리아는 현재 상기의 기술들을 활용하여 '간'이라는 표적 장기에 유전체를 편집하는 기술을 연구하고 있다.
인텔리아의 주요 개발 파이프 라인 중 In vivo 파이프라인으로는 1) 가족성 트랜스티레틴 아밀로이드증 (hATTR) 치료제 NTLA-2001 이 현재 글로벌 1상 진행 중이며 올해 말 첫 데이터를 공개할 예정이다. 두번째 파이프라인은 2) 유전성 혈관부종(HAE) 치료제로 NTLA-2002는 현재 전임상을 마쳐 2021년 하반기 IND 제출 예정이다.
Ex vivo 파이프라인으로는 현재 1/2상 진행 중인 3) 겸상적혈구질환 치료제 OTQ923과 하반기 IND 제출 예정인 4) 급성 골수성 백혈병 (AML) 치료제 NTLA-5001 등을 보유하고 있다.
In-Vivo 파이프라인
자체 개발 LNP로 간 특이적 Crispr 기술 적용
인텔리아의 in vivo 파이프라인은 유전자 편집을 진행한 Cas9 mRNA와 타겟 유전자로 안내할 guide RNA를 LNP (Lipid Nano Particle; 지질 나노입자)에 담아 정맥 주사를 통해 각 세포 내에 전달함으로써 간 내의 타겟 유전자를 knock-out (제거, 유전자가 작동하지 않도록 하는 기술)시키는 작용을 한다.
LNP는 기본 적으로 혈중 ApoE와 결합하여 각 세포 표면의 ApoE 수용체를 통해 주로 간 내에 유입되지만 지나친 축적으로 인한 독성문제가 존재했는데, 인텔리아는 지질구조에 에스테르 링크(labile ester linkages)를 연결 해 생분해성을 강화하여 동물임상에서 기존 LNP 대비 1/4 수준의 반감기를 달성했다.
또한, 낮은 수준의 off-target (표적 이탈)효과를 보여주며 의도하지 않은 유전자 편집으로 인한 부작용을 방지하는 데 성공했다(Fine et al., Cell, 2018). 향후 간 내 세포 타겟에서 골수, 중추신경계 등으로 in vivo 파이프라인 타겟을 확장할 예정이다.
NTLA-2001, 기존의 유전자 치료제를 뛰어넘는 Crispr 기반의 치료제로 연내 임상 1상 결과 발표 예정
NTLA-2001은 유전성 트랜스티레틴 아밀로이드증 (hATTR) 치료제로 4Q20 첫 환자 투약을 시작으로 글로벌 임상 1상 진행 중 (리제네론과 공동 개발 중)이며, 현시점에서 환자에게 투여된 최초의 Crispr 기반 치료제로 first-in-class 의약품을 목표로 한다. ATTR (Transthyretin Amyloidosis)은 트랜스티레틴 유전자의 돌연변이로 인해 간에서 잘못 접힌 트랜스티레틴 단백질이 생성돼 각종 신경손상과 심장 근육의 이상을 일으키는 질환이다. 전 세계에 5만여 명의 환자가 존재하는 것으로 알려져 있으며, 증상 발현 이후 기대수명이 평균 2-15년으로 현재까지 만성적인 치료가 유일한 옵션인 만큼 영구적 치료에 대한 unmet needs가 존재하는 질환이다.
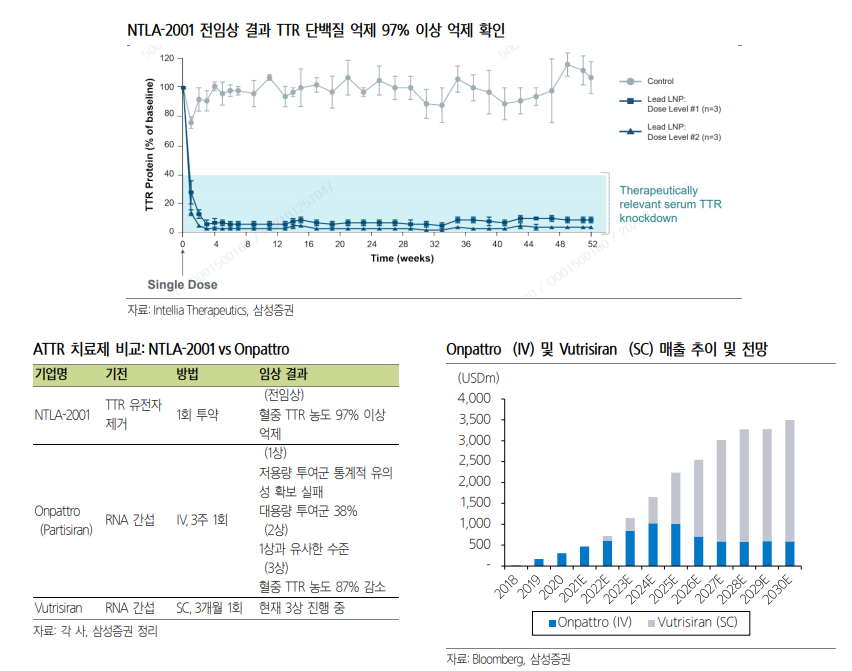
NTLA-2001은 간 내의 TTR 유전자 돌연변이를 편집하여 영장류 대상 전임상에서 첫 투여 이후 혈청 내 TTR 단백질을 97% 이상 억제하는 효과를 보이며 PoC를 입증한 바 있다. 사람 대상 임상 1상에서는 4 가지 용량별 투약 내성 시험 코호트와 hATTR로 인한 신경다발증 및 심근증 환자들에 대핚 단일용량 코호트 총 두 파트로 시험을 진행하여 1차 목표로 안전성과 약물 내약성을, 2차 목표로 약효 확인 예정으로, 올해 말 첫 데이터를 공개할 것으로 전망된다.
올해 6월 26일 미국 리제네론과 함께 크리스퍼 기술을 적용한 희귀 심혈관 질환인 트랜스티래틴아밀로이드(ATTR) 치료제 후보 'NTLA-2001'의 임상 1상 중간결과 해당 후보물질이 질병을 일으키는 단백질 생성을 크게 줄였다는 결과를 공개했다. 이번 인텔리아와 리제네론의 임상시험은 생체 내(in vivo) 환경에서 크리스퍼 기술을 적용한 첫 임상시험 결과다.
이 발표로 지금은 주가가 많이 하락했지만 인텔리아를 필두로 크리스퍼 치료 기업들의 주가가 급등했다.
https://www.news1.kr/articles/?4361360
美인텔리아. 크리스퍼 적용 첫 임상소식에 주가 2배 넘게 급상승
사실 앞에 겸손한 민영 종합 뉴스통신사 뉴스1
www.news1.kr
NTLA-2002, 2H21 FDA에 임상 1상 IND 신청 예정
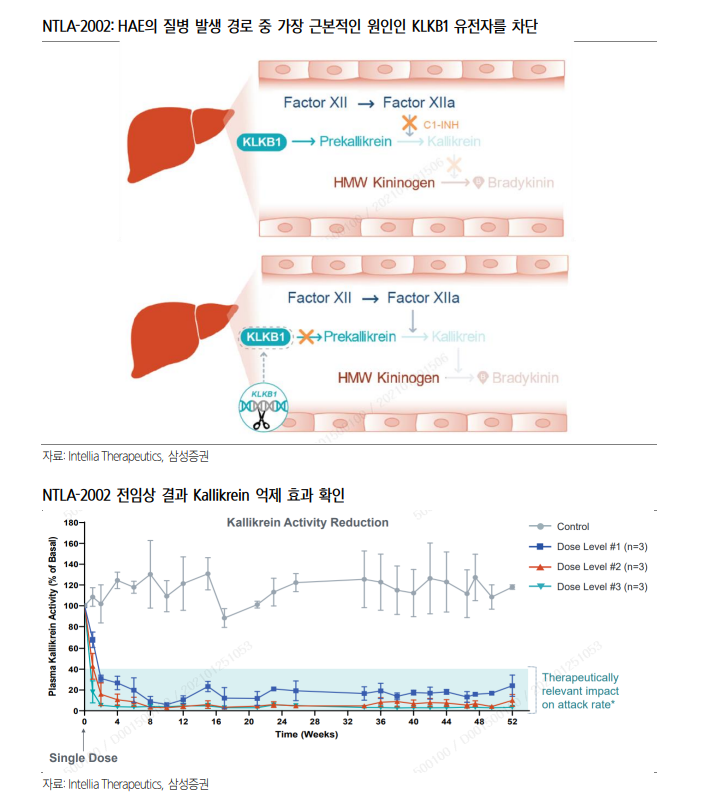
NTL-2002는 유전성 혈관부종 (HAE) 치료제로 2H21에 IND 제출하였다. 유전성 혈관부종 (Hereditary angioedema)은 신체 다양한 부위에 7-14일에 한번 꼴로 심각한 부종이 발생하는 질환으로, 전 세계에 약 5만 명당 한 명 꼴로 발생한다. NTLA-2002는 LNP 안에 KLKB1 유전자에 도달하게 할 guide RNA와 Cas9 mRNA를 같이 담아 보내 KLKB1 유전자를 knock-out 하여 붓기를 유발하는 브래디키닌 (bradykinin) 단백질의 발생 경로를 원천적으로 차단하는 역할을 한다.
기존에 치료제로 쓰이는 C1-에스트라제 억제제의 경우 Kallikrein의 전 단계인 Prekallikrein의 변환 과정을 차단하지만 원인 유전자를 근본적으로 차단하지 못해 지속적인 투약을 통해서만 증상을 억제할 수 있다. 또 다른 치료제인 브래디키닌 수용체 길항제의 경우 부종을 일으키는 단백질인 브래디키닌 수용체에 달라붙어 단백질의 발현을 막지만 역시 근본적인 치료법은 되지 못하는 상황이다. NTLA2001은 동물임상에서 질환의 직접적 원인인 Kallikrein을 효과적으로 억제하는 것으로 확인되었으며, 기존 치료제들과 달리 한 번의 투여를 통해 기존 치료방법 대비 장기적인 치료 효과를 가져올 것으로 기대된다.

Ex-Vivo 파이프라인
OTQ923
겸상적혈구질환 치료제로, 현재 임상 1/2상 진행 중 (노바티스와 협력)으로 2023년 임상 종료 예정이다. 유전자 가위를 이용하여 tgTCR (유전자이식 T세포 수용체)의 발현율을 높임으로써 이식편대 숙주 증후군의 위험을 낮추고 높은 효능의 세포 생산이 가능하다.
NTLA-5001
WT1 (Wilms’ Tumor1) 타겟 급성 골수성 백혈병 (AML) 치료제이다. 급성 골수성 백혈병은 미국에서는 연간 2만 명, 전 세계적으로는 연간 4만 명 이상의 환자가 발생하는 질환으로, 5년 생존율이 30% 미만인 희귀병이다. 유전자 조작된 T세포 수용체 (TCR)을 삽입함으로써 보다 균질한 T세포 수용체를 통해 AML 모세포의 90% 이상에서 과발현 되는 항원인 WT1을 정밀하게 타겟할 수 있다. 하반기에 진행될 임상 1 상의 대상자들은 1차 치료 후에도 지속적/반복적 증상을 겪는 AML 환자들로, 혈액암 외에도 폐암, 유방암 등 다수의 고형암에서도 과발현 된다는 연구결과가 존재하는 만큼 향후 적응증 확장 가능성을 기대할 수 있다.
4. NTLA, 인텔리아 테라퓨틱스 Risk Factor
1. 심화되고 있는 경쟁
유전자 치료 마켓은 워낙 시장 잠재력도 뛰어나고 향후 발전 가능성이 굉장히 높기 때문에 인텔리아를 포함한 많은 기업들이 시장에 진출하고 있다. NTLA, CRSP, EDIT와 현재는 유전자 치료 3대장 기업으로 불리지만, 이러한 경쟁 속에서 어떻게 살아남느냐가 굉장히 중요한 투자 리스크 중 하나가 될 것이다.
2. 임상실험 Risk
인텔리아도 유전자 치료 기업이지만, 결국 바이오 기업이다. 최근 좋은 임상결과에 웃을 수 있었던 만큼, 조금의 부작용과 부정적인 결과가 나오더라도 주가는 급락할 수 있다. 유전자 치료의 경우 과학의 영역과 창조주의 영역에 걸쳐있다. 유전자를 임의로 편집하였을 때의 결과는 미개척지의 영역이므로 각 치료제의 임상결과에 따라 엄청난 변동성을 동반할 것이다.
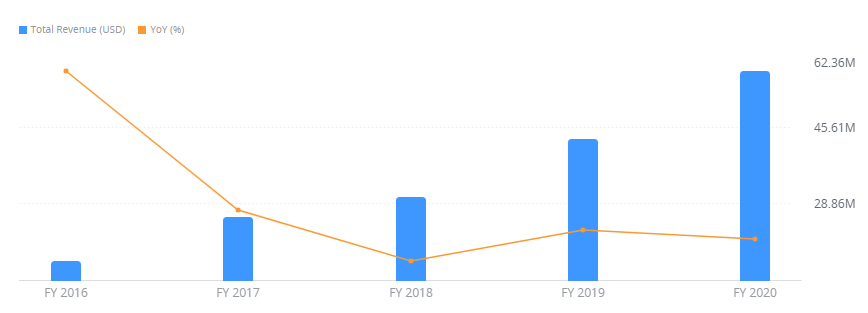
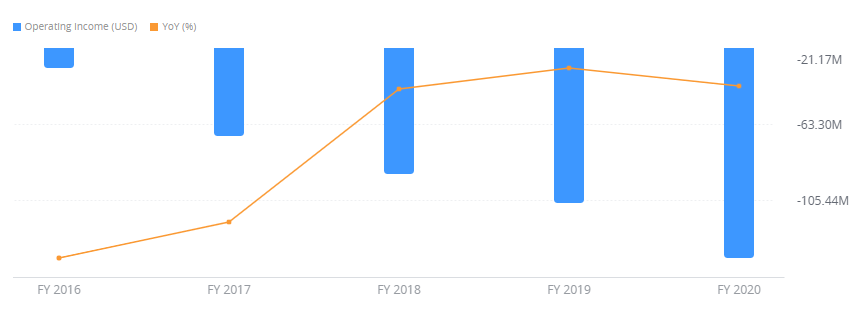
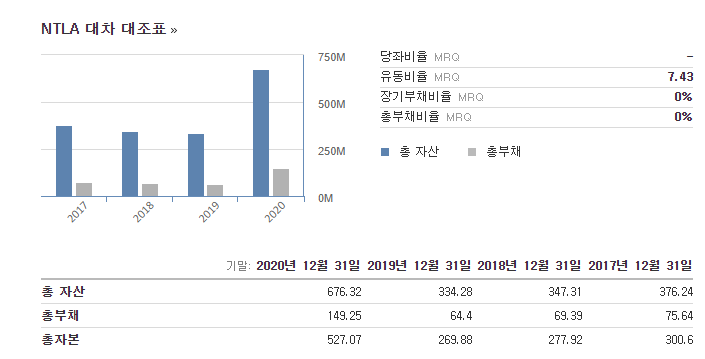
5. 재무제표
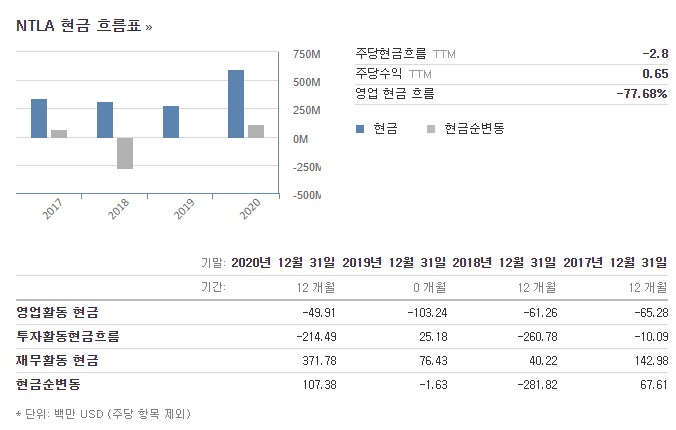
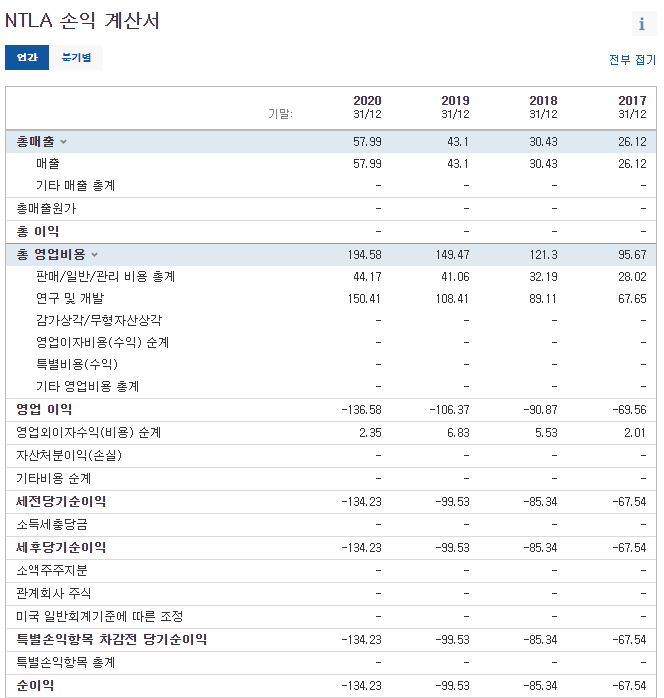
6. NTLA, 인텔리아 투자가치 및 투자 아이디어
재무제표의 경우 분석이 무의미할 정도로 매출보다 더 많은 금액을 신규 기술 연구 및 개발에 투자하고 있는 상황이다. 바이오 기업 특성상, 유의미한 상용화 치료제 개발이 되기 전까지 버틸 수 있는 자본과 투자자들의 관심을 끌만한 유의미한 결과를 지속적으로 발표하는 것이 중요하다. 현재 인텔리아의 경우 현금흐름 및 부채비율면에서 건전한 재무상태를 유지하고 있는 것은 긍정적으로 볼 수 있다.
앞으로 개발되는 임상실험 결과에도 주목해야하지만, 기술이 개발되기 전까지 기업의 자본이 마르지 않는지 체크하는 것도 중요할 것이며 경쟁사인 CRSP, EDIT 등 다른 유전자 편집 기술 기업의 성장성 및 임상결과에도 주목해야 한다.
일반 투자자는 물론 생명공학이나 의학을 전공하여 크리스퍼 관련 기업의 기술력에 대한 전반적인 이해와 임상실험 스케쥴을 꽤 차고 있더라도 바이오 기업 특성상 임상실험 결과에 따르는 변동성을 예측하고 대응하기에는 어려울 것으로 판단된다.

그럼에도 불구하고, 유전자 편집 치료 시장은 연평균 17.2% 성장하며 성공적인 치료법이 개발되었을 경우 그 잠재력은 무궁무진하다. 이론상 유전자 편집을 통해 난치병과 불치병 모두 치료할 수 있으며 이 기술은 적용되기까지 상당히 많은 시간이 걸리겠지만, 해당 기술은 단연코 세상을 바꿀 기술 중 하나이다.
인텔리아 테라퓨틱스는 사람들이 삶에서 가장 중요시 여기는 그것, '생명의 연장'에 기여하는 기업 중 하나라고 생각하고 미래의 기술에 대한 희망과 바이오 기업의 변동성을 버텨낼 용기가 있는 투자자라면 투자해볼 만한 기업이라 생각된다.
# 함께 보면 좋은 글
* 유전자 분석 기업 : 인비테(인바이테)
https://open.kakao.com/o/gLcMA3Pd
YoungH의 경제적 자유를 위한 모든 것
#미국주식 #해외주식 #국내주식 #부동산 #가치투자 #장기투자 #젊은부자 #조기은퇴 #경제적자유 #기업분석
open.kakao.com
함께 경제적 자유를 쟁취할 분들을 위한 오픈 카톡방입니다. 경제뉴스 및 주식 시황 그리고 투자 인사이트 및 아이디어 등을 서로 공유하면서 함께 성장하고자 하는 목적으로 운영중에 있습니다. 주식뿐만 아니라 부동산, 사업, 등 다양한 주제로 소통해나갈 예정입니다.
#참여코드 : YOUNGH
'투자노트 > 미국 주식' 카테고리의 다른 글
| [에디타스 메디슨, EDIT] 유전자 가위 특허 전쟁, 유전자 가위, 유전자 편집 치료 혁신 기업 EDIT 주가 및 기업분석 (0) | 2021.11.04 |
|---|---|
| [크리스퍼 테라퓨틱스, CRSP] ARK 캐시우드가 선택한 노벨 화학상 유전자 가위, 유전자 편집 치료 혁신 기업 CRSP 주가 및 기업 분석 (0) | 2021.10.25 |
| [인비테, NVTA] 유전자 데이터 플랫폼 기업 인비테 인바이테 INVITAE 주가 및 기업분석 (0) | 2021.07.12 |
| [브이룸, VRM] 미국 온라인 중고차 중개 플랫폼 브이룸(VROOM) 주가 및 기업분석 (0) | 2021.06.20 |
| [카바나, CVNA] 미국 중고차 중개 플랫폼의 게임체인저 카바나(CARVANA) 주가 및 기업분석 (0) | 2021.06.14 |